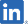| 製品名(開発コード) | 適応/効果 | 地域 | 非臨床 | 臨床試験 | 申請 | 承認/上市 | 進捗状況 | 提携先 (対象地域) |
||
|---|---|---|---|---|---|---|---|---|---|---|
| 第Ⅰ相 | 第Ⅱ相 | 第Ⅲ相 | ||||||||
|
エピシル® 口腔用液(SP-03) MORE INFO |
口内炎疼痛緩和 <医療機器> | 日本 |
|
|
|
|
2018年販売開始 |
Meiji Seika ファルマ (日本)
(中国)
(韓国) |
||
| 中国 |
|
|
|
|
2019年販売開始 | |||||
| 韓国 |
|
|
|
|
2020年販売開始 | |||||
SP-03
当社は、SP-03の開発事業化にかかる独占的ライセンス契約をCamurus AB(以下 Camurus)と、2015年3月に日本及び中国権利、また2018年8月に韓国権利につきそれぞれ締結しました。
SP-03は、口腔内病変の被覆及び保護を目的とする非吸収性の液状機器です。口腔粘膜に適量を適用すると数分以内に口腔粘膜の水分を吸収してゲル状になり、物理的バリアを形成することにより、口内炎で生じる口腔内疼痛を管理及び緩和します。
SP-03はCamurusの特許技術であるFluidCrystal®(FluidCrystal® は2013年に開催されたCPhI Worldwideで「Best innovation in formulation」を受賞しています。)を用いて開発されました。適用後、数分以内で効果的に口腔内の局所疼痛を緩和し、その効果が8時間程度持続することが臨床的に示されています*。SP-03はがん等の化学治療や放射線療法を受けている患者の生活の質(クオリティ オブ ライフ)の改善に貢献するための、持ち運び可能なポケットサイズの医療機器です。
* Hadjieva, T et al. Treatment of oral mucositis pain following radiation therapy for head-and-neck cancer using a bioadhesive barrier-forming lipid solution. Support Care Cancer 2014, 22:1557–1562
開発状況: 販売開始済(日本・中国・韓国)
日本では2017年7月に当局より承認を取得し、2018年5月に国内独占販売権導出先であるMeiji Seika ファルマ社より販売が開始されました。
中国では2019年2月に当局より承認を取得し、同年7月に販売を開始しました。 中国販売においては、2025年3月よりChangchun GeneScience Pharmaceutical Co.,Ltd.が販売活動を行っております。
韓国では2019年10月に当局より承認を取得し、2020年9月に販売権導出先であるSynex社より販売が開始されました。